化学を学ぶ上で多くの人がつまずきやすいテーマ、「ギブスエネルギーと化学平衡」について解説します。
教科書を見ると数式がたくさん並んでいて、アレルギーを起こしそうになる方も多いかもしれません。しかし、数式の意味と全体像のイメージさえ掴んでしまえば、化学反応がどちらに進むのかが手に取るようにわかるようになります。
この記事でしっかりと基本を押さえていきましょう。
1. ギブスエネルギーとは
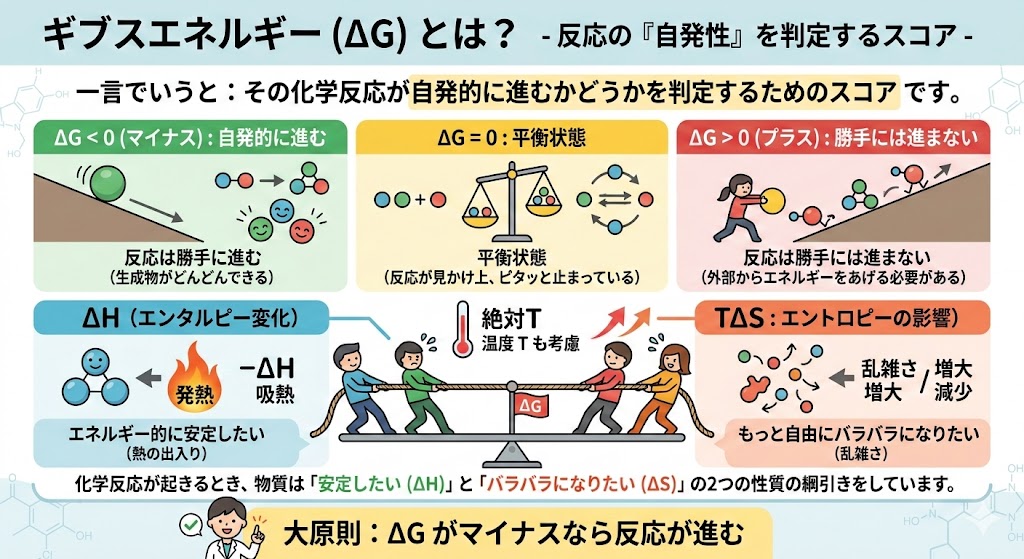
一言でいうと、ギブスエネルギーとは「その化学反応が自発的に進むかどうかを判定するためのスコア」です。
化学反応が起きるとき、物質は「エネルギー的に安定したい(エンタルピー $H$)」という性質と、「もっと自由にバラバラになりたい(エントロピー $S$)」という2つの性質の綱引きをしています。
この綱引きの結果を、温度($T$)も考慮してまとめたのが次の式です。$$\Delta G = \Delta H – T\Delta S$$
計算した結果、$\Delta G$ がプラスになるかマイナスになるかで、その反応の運命が決まります。
- $\Delta G < 0$ (マイナス)の場合:反応は勝手に進む(生成物がどんどんできる)
- $\Delta G > 0$ (プラス)の場合:反応は勝手には進まない(外部からエネルギーをあげる必要がある)
- $\Delta G = 0$ の場合:平衡状態(反応が見かけ上、ピタッと止まっている)
まずは「$\Delta G$ がマイナスなら反応が進む」という大原則を頭に入れておきましょう。
2. 2つの「標準ギブスエネルギー」の違い
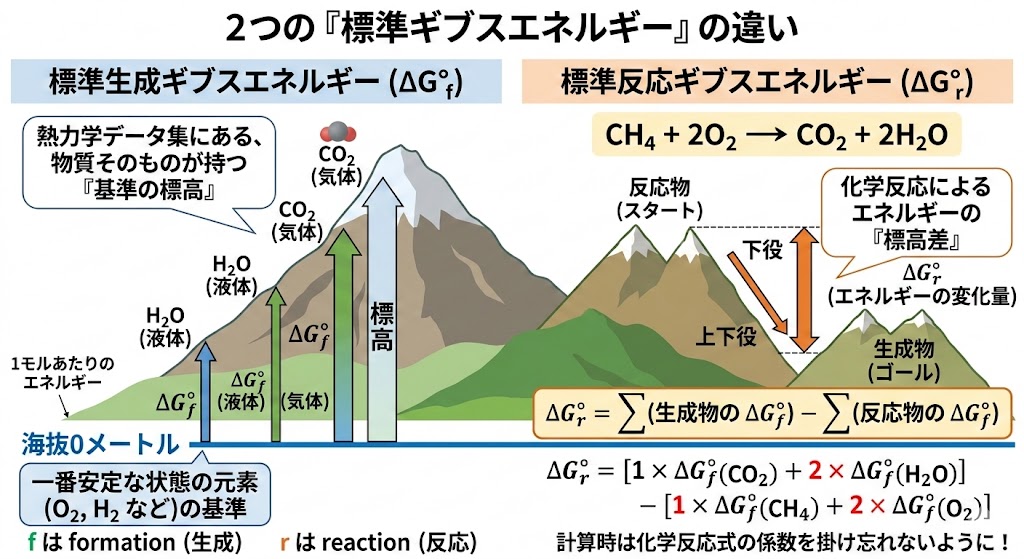
勉強を進めると、「標準生成ギブスエネルギー」と「標準反応ギブスエネルギー」という似たような言葉が出てきます。ここを混同すると理解がこんがらがってしまうので、明確に区別しましょう。
山の標高をイメージすると分かりやすいです。
標準生成ギブスエネルギー($\Delta G_f^\circ$)
これは、熱力学データ集などの表に載っている、各物質が持っている基準となる絶対的な数値(山の標高)です。($f$ は formation:生成 を意味します)
一番安定な状態の元素($O_2$ や $H_2$ など)を基準の「海抜0メートル」とし、そこから特定の化合物を1モル作ったときのエネルギーの高さを表します。
標準反応ギブスエネルギー($\Delta G_r^\circ$)
一方こちらは、特定の化学反応が起きたときの、反応全体でのエネルギーの変化量(スタートとゴールの標高差)です。($r$ は reaction:反応 を意味します)
化学反応式の通りに反応が進んだとき、ゴール(生成物)の総標高から、スタート(反応物)の総標高を引いて求めます。$$\Delta G_r^\circ = \sum (\text{生成物の } \Delta G_f^\circ) – \sum (\text{反応物の } \Delta G_f^\circ)$$
実際の計算では、表で与えられた「生成(標高データ)」を使って、自分で「反応(どれだけ下ったか・登ったかの標高差)」を求めることがよくあります。計算時は化学反応式の係数(モル数)を掛け忘れないように注意してくださいね。
3. 反応を予測する公式$\Delta G^\circ = -RT \ln K$
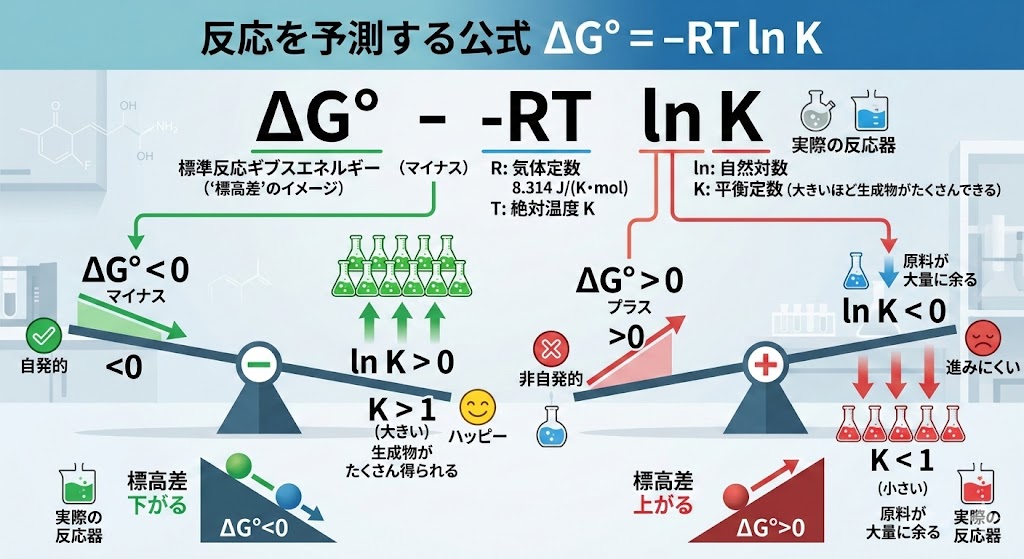
さて、先ほど求めた標高差である $\Delta G^\circ$ (標準反応ギブスエネルギー)を使って何をするかというと、実際の反応器の中でガスや生成物がどれくらい作られるか(平衡定数 $K$)を予測します。
それを繋ぐのが、以下の最重要公式です。$$\Delta G^\circ = -RT \ln K$$
- $R$ : 気体定数(8.314 J/(K・mol))
- $T$ : 絶対温度(K)
- $K$ : 平衡定数(大きいほど生成物がたくさんできる)
- $\ln$ : 自然対数
式の右辺にマイナス($-$)がついているのがポイントで、以下のようなシーソー関係が成り立ちます。
- $\Delta G^\circ$ がマイナス($<0$)のとき$\ln K$ はプラスになり、$K > 1$ となります。つまり、反応が自発的に進んで、生成物がたくさん得られるハッピーな状態です。
- $\Delta G^\circ$ がプラス($>0$)のとき$\ln K$ はマイナスになり、$K < 1$ となります。反応は進みにくく、せっかく入れた原料が大量に余ってしまう状態です。
4. 自然対数(ln)のイメージ
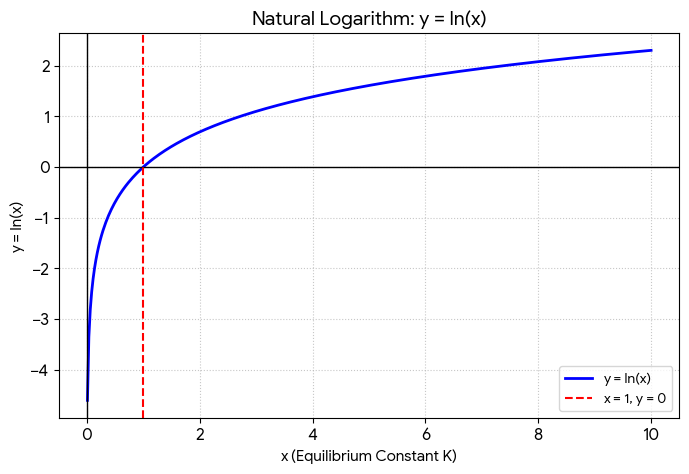
数式の中に $\ln$ が出てくると難しく感じますが、ここでは単なる「フィルター」だと思ってください。
「1」という数字を基準にして、数値をプラスとマイナスに振り分ける便利なツールです。
- 平衡定数 $K = 1$ のとき、$\ln K = 0$ になります。これが平衡のど真ん中です。
- $K$ が1より大きい(生成物が多い)と、$\ln K$ はプラスの数字になります。
- $K$ が0から1の間(生成物が少ない)だと、$\ln K$ はマイナスの数字になります。
難しく考えすぎず「1より大きいか小さいかを判定しているんだな」くらいに捉えておけば大丈夫です。
5. まとめ
アンモニア合成(ハーバー・ボッシュ法)などを工場で行う際、いかにして平衡定数 $K$ を大きくするかが、製品を効率よく作るための要となります。
化学プラントのエンジニアは、「この反応は発熱反応だから、温度 $T$ を下げたほうが $\Delta G$ がマイナスになって生成物側にズレるな」といった判断を、勘ではなく、今回紹介した数式を使って定量的に計算・設計しています。
このように、ギブスエネルギーは単なる机上の空論ではなく、私たちの生活を支える化学産業の重要な基盤となっています。まずは各用語の違いと、公式の結びつき(シーソー関係)をしっかりイメージして、化学反応の面白さを味わってみてください!
 化学プラント大全
化学プラント大全 
