化学や物理化学を学んでいると、必ず出会う「ドルトンの法則」と「ラウールの法則」。 それぞれ独立した法則として覚えがちですが、実は「気液平衡」という現象において、この2つはがっちりと手を結びます。
今回は、気相と液相をつなぐ架け橋となる、この2つの法則の関係性について分かりやすく解説します。
ドルトンの法則(気相の世界のルール)
まずは気体の世界のおさらいからです。
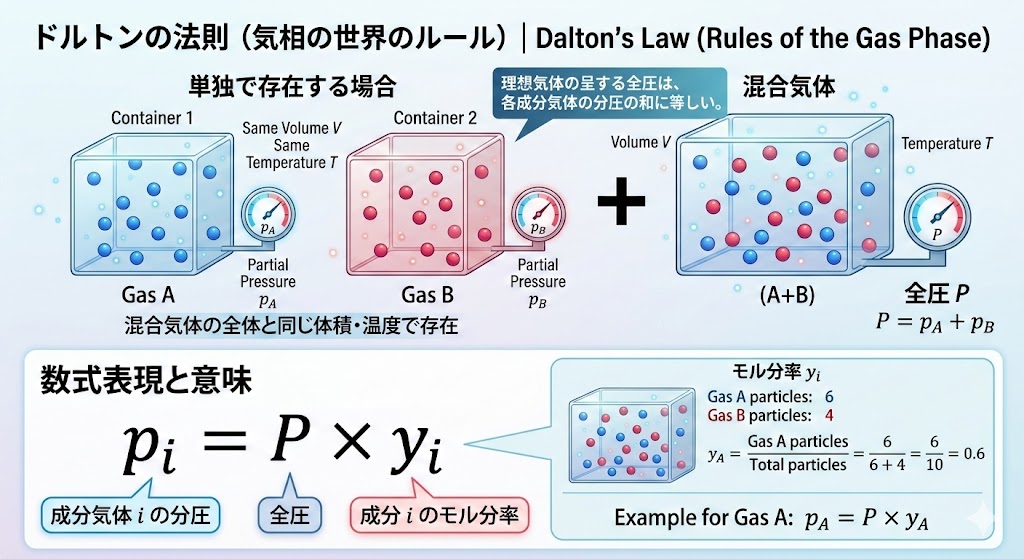
混合気体中のある成分気体のみが、単独で混合気体全体と同じ体積に同じ温度で存在すると考えたときに呈する圧力をその成分気体の分圧といいます。これに対して、混合気体全体が呈する圧力を全圧といいます。また、理想気体とみなせる混合気体の呈する全圧は、各成分気体の分圧の和に等しい。これをドルトンの法則といいます。
これを数式で表すと、気相中のある成分 $i$ の分圧 $p_i$ は、全圧 $P$ と気相中のモル分率 $y_i$ を用いて次のように書けます。$$p_i = P \times y_i$$
ラウールの法則(液相から気相へのアプローチ)
次に液体の世界からの視点です。
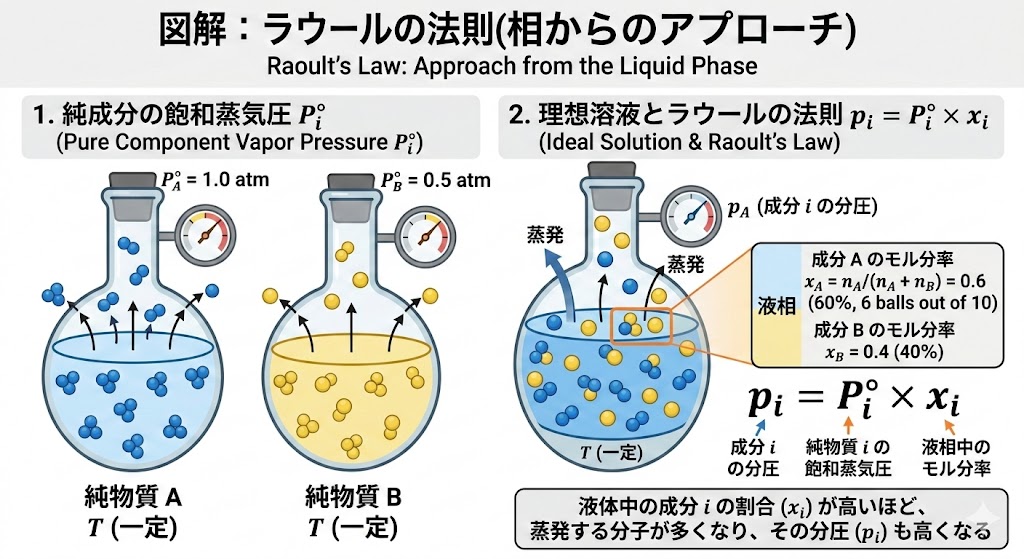
理想溶液において、ある成分 $i$ の分圧 $p_i$ は、その温度における純物質 $i$ の飽和蒸気圧 $P^{\circ}_i$と、液相中のモル分率 $x_i$ の積に等しいという法則があります。これがラウールの法則です。$$p_i = P^{\circ}_i \times x_i$$
液体の中にどれくらいの割合でその成分が含まれているか(モル分率 $x_i$)と、その物質本来の蒸発しやすさ(飽和蒸気圧 $P^{\circ}_i$)の掛け算で、実際に生じる圧力が決まるというわけです。
2つの法則が交わる場所:気液平衡
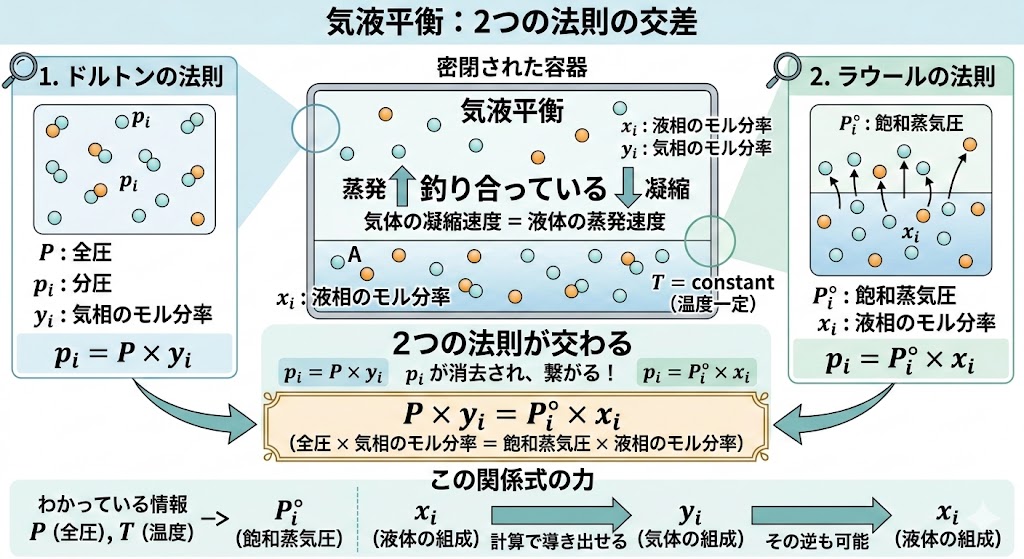
密閉された容器の中で、液体の蒸発と気体の凝縮が釣り合っている状態を「気液平衡」と呼びます。 この平衡状態において、いよいよ2つの法則が結びつきます。
ドルトンの法則で表される「気相の分圧」と、ラウールの法則で表される「液相から生じる分圧」は、平衡状態では全く同じもの(等しい圧力)になります。
したがって、先ほどの2つの式から $p_i$ を消去して繋ぎ合わせると、次のような美しい関係式が得られます。$$P \times y_i = P^{\circ}_i \times x_i$$
(全圧 × 気相のモル分率 = 飽和蒸気圧 × 液相のモル分率)
この関係式は非常に強力です。 理想的な系において、全圧 $P$ と温度(温度が決まれば飽和蒸気圧 $P^{\circ}_i$ も決まります)がわかっていれば、液体の組成 $x_i$ から気体の組成 $y_i$ を計算で導き出すことができるのです。もちろんその逆も可能です。
具体的な計算例で確認してみよう
理想溶液として振る舞うベンゼン(成分A)とトルエン(成分B)の混合液を例に、具体的な数値を当てはめて計算してみましょう。
ある一定の温度において、純粋なベンゼンの飽和蒸気圧 $P^{\circ}_A$ が 100 kPa、純粋なトルエンの飽和蒸気圧 $P^{\circ}_B$ が 40 kPa だとします。 この時、液相中のベンゼンのモル分率 $x_A$ が 0.4、トルエンのモル分率 $x_B$ が 0.6 である混合液が、気液平衡状態にあるとします。
この時の「全圧 $P$」と「気相中のモル分率 $y_A, y_B$」を求めてみましょう。
ステップ1:ラウールの法則から、各成分の分圧を求める
ベンゼンの分圧 $p_A = P^{\circ}_A \times x_A = 100 \text{ kPa} \times 0.4 = 40 \text{ kPa}$
トルエンの分圧 $p_B = P^{\circ}_B \times x_B = 40 \text{ kPa} \times 0.6 = 24 \text{ kPa}$
ステップ2:ドルトンの法則から、全圧を求める
全圧 $P = p_A + p_B = 40 \text{ kPa} + 24 \text{ kPa} = 64 \text{ kPa}$
ステップ3:ドルトンの法則を変形し、気相中のモル分率を求める
ベンゼンの気相モル分率 $y_A = p_A / P = 40 \text{ kPa} / 64 \text{ kPa} = 0.625$
トルエンの気相モル分率 $y_B = p_B / P = 24 \text{ kPa} / 64 \text{ kPa} = 0.375$
計算の結果、液相ではベンゼンの割合が 0.4 だったのに対し、気相ではベンゼンの割合が 0.625 に増えていることがわかります。ベンゼンの方が飽和蒸気圧が高く(蒸発しやすく)、気相により多く集まるという直感的な理解とも一致しますね。
シミュレーターで体感
ドルトンの法則とラウールの法則の計算例を体験
スライダーを動かして、液体の組成(xA)や各物質の蒸発しやすさ(飽和蒸気圧)が変化したときに、気体の組成(yA)がどう変わるか観察してみましょう。
pA = 100 × 0.40 = 40 kPa
pB = 40 × 0.60 = 24 kPa
P = 40 + 24 = 64 kPa
yA = 40 / 64 = 0.625
yB = 24 / 64 = 0.375
実際の化学プラントへの応用
このシンプルな関係式は、化学プラントのプロセス設計において欠かせないものです。蒸留塔やフラッシュドラムといった、気体と液体を分離する装置の物質収支や平衡計算は、すべてここからスタートします。
ただし、現実の世界の液体は完全に理想的な振る舞いをするとは限りません。 実際のプロセス設計では、理想系からのズレを補正するために「活量係数 $\gamma_i$」というものを導入した修正ラウールの法則がよく用いられます。$$P \times y_i = \gamma_i \times P^{\circ}_i \times x_i$$
このように少し複雑にはなりますが、ベースとなる考え方はドルトンの法則とラウールの法則の結合に他なりません。
気相と液相、それぞれの視点を持った法則が「平衡」というキーワードで一つに繋がる。化学熱力学の面白さを感じられるポイントではないでしょうか。
 化学プラント大全
化学プラント大全 
